Explicamos o que é termodinâmica e em que consiste um sistema termodinâmico. Além disso, quais são as leis da termodinâmica.
O que é Termodinâmica?
É chamada de termodinâmica (do grego garrafa térmica“calor” e dínamos“poder, força”) ao ramo da física que estuda as ações mecânicas do calor e outras formas similares de energia. O seu estudo aborda os objetos como sistemas macroscópicos reais, através do método científico e do raciocínio dedutivo, prestando atenção a variáveis extensas como entropia, energia interna ou volume; bem como variáveis não extensivas como temperatura, pressão ou potencial químico, entre outros tipos de grandezas.
No entanto, a termodinâmica não oferece uma interpretação das magnitudes que estuda, e seus objetos de estudo são sempre sistemas em estado de equilíbrio, ou seja, aqueles cujas características são determináveis por elementos internos e não tanto por forças externas que sobre eles atuam. Por esta razão, considera-se que a energia só pode ser trocada de um sistema para outro na forma de calor ou trabalho.
O estudo formal da termodinâmica começou graças a Otto von Guericke em 1650, um físico e jurista alemão que projetou e construiu a primeira bomba de vácuo, refutando Aristóteles e sua máxima de que “a natureza abomina o vácuo” com suas aplicações. Após esta invenção, os cientistas Robert Boyle e Robert Hooke aperfeiçoaram seus sistemas e observaram a correlação entre pressão, temperatura e volume. Assim nasceram os princípios da termodinâmica.
Veja também: Calor específico
sistema termodinâmico

Entende-se por sistema termodinâmico uma parte do universo que, para fins de estudo, está conceitualmente isolado do resto e tenta-se compreendê-lo de forma autônoma. Tome nota das formas como a energia muda ou é preservada e, ao mesmo tempo, as suas trocas de matéria e/ou energia com o ambiente ou com outros sistemas semelhantes (se houver). É, portanto, um método de estudo da termodinâmica.
O principal critério de classificação destes sistemas baseia-se no seu grau de isolamento do meio ambiente, distinguindo assim entre:
- Sistemas abertos. Aqueles que trocam livremente energia e matéria com o ambiente, como fazem os sistemas mais conhecidos na vida cotidiana. Por exemplo: um carro. Você fornece combustível e ele devolve gases e calor ao meio ambiente.
- Sistemas fechados. Aqueles que trocam energia com o meio ambiente, mas não importam. É o que acontece com um recipiente fechado, como uma lata, cujo conteúdo permanece inalterado, mas perde calor com o tempo, dissipando-o no ar circundante.
- Sistemas isolados. Aqueles que, até certo ponto, não trocam energia nem matéria com o meio ambiente. É claro que não existem sistemas perfeitamente isolados, mas existem até certo ponto: uma garrafa térmica contendo água quente manterá sua temperatura por um tempo, o suficiente para permanecer isolada por um tempo.
Leis da termodinâmica

A termodinâmica é regida pelo que está estabelecido em seus quatro princípios ou leis fundamentais, formulados por diversos cientistas ao longo da história desta disciplina. Esses princípios ou leis são:
- Primeiro princípio, ou Lei da Conservação da energia. Estabelece que a quantidade total de energia em qualquer sistema físico isolado de seu ambiente será sempre a mesma, embora possa ser transformada de uma forma de energia em muitas outras diferentes. Em poucas palavras: “A energia não pode ser criada nem destruída, apenas transformada”.
- Terceiro princípio, ou Lei do zero absoluto. Dita que a entropia de um sistema levado ao zero absoluto será sempre uma constante definida. Isso significa que ao atingir o zero absoluto (-273,15° C ou 0 K), os processos dos sistemas físicos param e a entropia tem um valor mínimo constante.
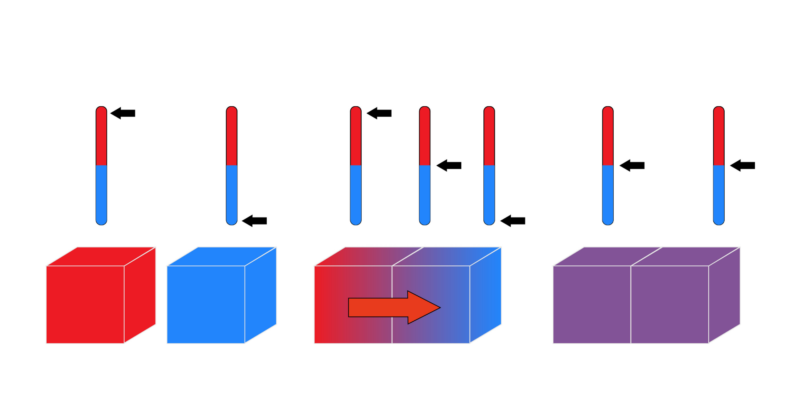
- Princípio zero ou Lei do equilíbrio térmico. É chamada de “lei zero” porque, embora tenha sido a última a ser postulada, os preceitos básicos e fundamentais que estabelece têm prioridade sobre as outras três leis. Ela determina que “se dois sistemas estão em equilíbrio térmico independentemente de um terceiro sistema, eles também devem estar em equilíbrio térmico entre si”.
Mais em: Leis da termodinâmica
Termodinâmica química
A termodinâmica química é um campo de estudo separado, focado na correlação entre calor e trabalho e reações químicas, tudo enquadrado no que é estabelecido pelos princípios da termodinâmica. Ou seja, é a aplicação das leis da termodinâmica, especialmente as duas primeiras, ao mundo das reações entre substâncias e compostos, para obter as chamadas “equações fundamentais de Gibbs”, que regem a forma como a energia química contida nos diferentes compostos muda e é transmitido, ou como o grau de entropia do universo aumenta cada vez que ocorre uma reação espontânea.
Referências
- “Termodinâmica” na Wikipedia.
- “As leis da termodinâmica em 5 minutos” (vídeo) em Quantum Fracture.
- “O que é termodinâmica?” em Laboratório de Física.
- “Conceitos básicos de termodinâmica” na Universidade do País Basco.
- “Termodinámica: curso acelerado de física” (video) en Crash Course.
- “Termodinâmica” na Enciclopédia Britânica.